Kaftrio (Trikafta) – Triple-Therapie für Mukoviszidose (CF)

Kaftrio (in den USA: Trikafta) ist ein CFTR-Modulator. CFTR-Modulatoren verbessern die Funktion des CFTR-Kanals und somit auch den Gesundheitszustand von Menschen mit Mukoviszidose. Kaftrio besteht aus den Wirkstoffen Tezacaftor, Elexacaftor und Ivacaftor. Auf dieser Seite beschreiben wir Wirkungsweisen, den aktuellen Stand der Forschung und geben Tipps für den Umgang mit Nebenwirkungen.
Für wen kann Kaftrio verordnet werden?
Mutation (Variante)
Kaftrio ist in Deutschland für CF-Patienten zugelassen, die zwei Jahre und älter sind und mindestens eine Nicht-Klasse-1-Mutation haben.
Auch wenn die Zulassung jetzt für ca. 90% der Menschen mit Mukoviszidose erfolgt ist, wirkt Kaftrio voraussichtlich nicht bei allen. Bestimmte Mutationen (z.B. I507del oder L227R) oder sogenannte komplexe Allele (also mehrere Mutationen auf einem Gen) können dazu führen, dass Kaftrio nicht wirkt. Ggf. ist ein sogenannter ex vivo Test sinnvoll, um vor der Einnahme des Medikamentes die Wirksamkeit zu überprüfen. Diese Testsysteme stehen aber noch nicht überall in Deutschland zur Verfügung.
Bei Menschen mit Mukoviszidose, die zwei Klasse-1-Mutationen haben, ist Kaftrio zwar nicht zugelassen. In seltenen Fällen kann aber trotzdem eine Wirksamkeit da sein. In solchen Fällen kann ein Einzelfallantrag (off-label) an die Krankenkassen gestellt werden. Informationen zu Klasse-1-Mutationen, bei denen Kaftrio im französischen Härtefallprogramm gewirkt hat, gibt der englische Originalartikel von Burgel et al. 2025.
Alter
Kaftrio ist aktuell für Patienten ab zwei Jahren zugelassen (Stand November 2023) und kann verordnet werden.
Wahrscheinlich wird Kaftrio in den nächsten Jahren auch für jüngere Kinder zugelassen werden; entsprechende klinische Studien laufen bereits.
Kaftrio auf einen Blick
- Was: CFTR-Modulator
- Zugelassen: ab 2 Jahren
- Mutationen: mindestens eine Nicht-Klasse-I-Mutation
Besonderheiten Ernährung
Ihre Ansprechpartnerin

Dr. Jutta Bend
Leitlinien / Neugeborenen-Screening
Tel.: +49 (0)228 98780-47
E-Mail: JBend(at)muko.info
CF-CTN Germany Coordination Team
Tel.: +49 (0)228 98780-43
E-Mail: CFCTN(at)muko.info
Welche Nebenwirkungen kann Kaftrio haben?
Die folgende Aufstellung ist lediglich eine Auswahl der Informationen. Alle bekannten Nebenwirkungen sind in der Packungsbeilage aufgeführt. Für weitere Informationen lesen Sie bitte die Packungsbeilage bzw. fragen Sie Ihren behandelnden Arzt.
Erst einmal vorweg: Grundsätzlich sind viele Nebenwirkungen vorübergehend und verschwinden nach einigen Wochen wieder. Einige Betroffene berichten z.B. von:
- (Bauch)schmerzen, Durchfall oder Verstopfung
Tipp: Flohsamenschalen können hier helfen. Dabei beeinträchtigt wohl eine Einnahme bei Durchfall direkt mit Kaftrio dessen Wirkung nicht, bei Verstopfung sollte man zwischen der Einnahme von Kaftrio und der Einnahme der Flohsamen etwa eine Stunde warten.
- Sekretzunahme in den Atemwegen und dadurch vermehrten Husten
Tipp: Viel Wasser trinken!
- Kopfschmerzen, Ohrenschmerzen und Schwindel, was auch auf die anfängliche Sekretzunahme zurückgeführt wird
- Erhöhtem Blutdruck
- Hypoglykämie, also einem Absinken des Blutzuckerspiegels
- Muskelbeschwerden/schlappe Arme und Beine
Tipp: Durch die Einnahme von Kaftrio scheinen viele Patienten deutlich fitter zu werden. Wenn dadurch direkt sehr viel mehr Sport gemacht wird, kann das zur Erhöhung bestimmter Blutwerte führen, die diese Beschwerden verursachen. Besprechen Sie das Thema vor Einnahmebeginn mit Ihrem Ambulanzarzt.
- Erhöhten Leberenzymwerten, die eine Belastung der Leber anzeigen.
- Hautausschlägen, vor allem bei Frauen, die hormonelle Verhütungsmittel einnehmen.
- Erhöhter Fruchtbarkeit bei Frauen! (bei Bedarf an Verhütung denken)
- Unerwünschter Gewichtszunahme u.a. durch Heißhunger.
Tipp: Vereinbaren Sie vor Therapiebeginn einen Termin mit einer Ernährungsberatung um ggf. Ihre Ernährungsgewohnheiten anzupassen. Bei vielen Patienten verändert sich auch der Salzbedarf oder der Bedarf an hochkalorischer Zusatznahrung.
- Auch psychische Probleme (z.B. Depressionen), insbesondere bei psychiatrischen Erkrankungen in der Vorgeschichte, können auftreten (meist innerhalb von drei Monaten nach Therapiebeginn). Man sollte nach Start mit einer Kaftrio-Therapie auf Anzeichen für depressive Verstimmungen, Suizidgedanken oder ungewöhnliche Verhaltensweisen achten und bei Auftreten solcher Symptome sofort einen Arzt aufsuchen. Bitte scheuen Sie sich auch nicht, Ihren Arzt nach einem geeigneten Ansprechpartner zu fragen.
Tipp: Notieren Sie sich alle Nebenwirkungen. Sprechen Sie mit Ihrem behandelnden Ambulanzarzt über die Nebenwirkungen. Die Nebenwirkungen sollten durch den Arzt bei der zuständigen Behörde (BfArM) gemeldet werden. Nur so ist eine Beobachtung der Nebenwirkungen aller (neuen) Medikamente möglich. Sie können diese auch selber melden.
Was muss bei der Einnahme von Kaftrio beachtet werden?
Dosierung
Die optimale Dosis von Kaftrio wurde in klinischen Studien untersucht und in der Zulassung genau festgelegt. Es gibt Standarddosierungen und genau definierte alternative Dosierungen für bestimmte Situationen, z.B. bei der gleichzeitigen Einnahme von Medikamenten, die Wechselwirkungen mit Kaftrio haben können oder bei eingeschränkter Leberfunktion. Welche Dosis individuell richtig, das schätzt der behandelnde Arzt/die behandelnde Ärztin ein. Aber von den in den Fachinformationen vorgegebenen Dosierungen darf nur in gut begründeten Ausnahmefällen abgewichen werden und auch nur dann, wenn die zuständige Krankenkasse einen entsprechenden Antrag genehmigt hat. Die Standarddosierungen finden sich in den jeweiligen Fachinformationen und sind wie folgt:
Erwachsene:
- morgens zwei (orange) Kaftrio-Tabletten (enthalten die Wirkstoffe Ivacaftor, Tezacaftor und Elexacaftor) und
- abends eine (hellblaue) Tablette Kalydeco (enthält den Wirkstoff Ivacaftor)
Kinder:
Für Kinder sind alters- und gewichtsabhängige Dosierungen vorgesehen. Das bedeutet, dass die Dosis bei Kindern mehrmals umgestellt werden muss, wenn eine Alters- oder Gewichtsgrenze erreicht wird. Das ist notwendig, damit das Medikament optimal wirken kann.
Kinder ab sechs Jahre:
Es gibt eine Kaftrio-Packung für Kinder mit der halben Erwachsenen-Dosis.
- Kinder über 30kg Körpergewicht: morgens zwei Kaftrio-Tabletten und abends eine Kalydeco-Tablette (Erwachsenen-Dosis)
- Kinder unter 30kg Körpergewicht: morgens zwei Kaftrio-Tabletten und abends eine Kalydeco-Tablette (halbe Erwachsenen-Dosis, Kinder-Packung)
Kinder zwei bis unter sechs Jahre:
Für Klein- und Vorschulkinder gibt es ein Granulat in zwei unterschiedlichen Dosierungen.
- Kinder zwischen 10 und 14 kg: morgens ein Beutel Granulat mit 60 mg Ivacaftor/40 mg Tezacaftor/80 mg Elexacaftor und abends ein Beutel Granulat mit 59,5 mg Ivacaftor
- Kinder mit 14kg und mehr: morgens ein Beutel Granulat mit 75 mg Ivacaftor/50 mg Tezacaftor/100 mg Elexacaftor und abends ein Beutel Granulat mit 75 mg Ivacaftor.
Dabei sollen etwa zwölf Stunden Abstand zwischen den Einnahmen eingehalten werden!
Bitte sprechen Sie unbedingt Ihren Arzt an, wenn Sie Nebenwirkungen bemerken, damit Sie gemeinsam mit Ihrem Arzt entscheiden können, was nun zu tun ist. Bitte ändern Sie nicht ohne Rücksprache die Dosis oder die Reihenfolge der Einnahme.

Einnahme mit fetthaltigen Nahrungsmitteln empfohlen
Die Einnahme soll mit einem fetthaltigen Nahrungsmittel erfolgen. Das ist wichtig, damit die Wirkstoffe ihre Wirkung entfalten können. Beispiele sind: ein Stück Käse, ein Glas Vollmilch, ein Stück Schokolade, ein fetthaltiger Joghurt, etwas Avocado, Hummus, Fleisch, öliger Fisch, Nüsse, Sojaprodukte, fetthaltige Getränke.
Eine Tasse Vollmilch oder eine Handvoll Nüsse reicht dabei vollkommen aus, um die Tabletten einzunehmen. Wenn Sie sonst kein großes Frühstück gewohnt sind, müssen Sie nicht wegen Kaftrio eine große fetthaltige Mahlzeit zu sich nehmen.
Ausgewogene Ernährung ist wichtig!
Da sich in der Vergangenheit gezeigt hat, dass Kaftrio zu einer deutlichen Gewichtszunahme führen kann, ist eine gesunde und ausgewogene Ernährung besonders wichtig. Wenn Sie vorhaben, mit einer Kaftrio-Therapie zu beginnen, ist eine Ernährungsberatung sinnvoll.
Deshalb ist Grapefruit tabu
Auf Speisen und Getränke, die Grapefruit enthalten, müssen Sie während der Behandlung mit Kaftrio leider verzichten. Inhaltsstoffe der Grapefruit können nämlich den Abbau von Kaftrio in der Leber hemmen, so dass die Bioverfügbarkeit von Kaftrio im Körper erhöht wird. Dies könnte durch die zu hohe „Dosis“ Nebenwirkungen verursachen.
Kaftrio/Kalydeco als Ganzes schlucken
Die Tabletten müssen im Ganzen geschluckt werden und dürfen vor dem Schlucken nicht zerkaut, zerdrückt oder zerbrochen werden, weil derzeit keine klinischen Daten vorliegen, die für andere Anwendungsarten sprechen.
Präparate speziell für Kinder
Kinder ab sechs Jahre: Für Kinder unter 30kg Körpergewicht gibt es eine andere Kaftrio-Packung mit Tabletten in niedrigerer Dosierung (halbe Erwachsenen-Dosis). Es werden dann trotzdem zwei Tabletten am Morgen genommen. Kinder über 30kg Körpergewicht bekommen dieselbe Dosierung wie Erwachsene und die bisher gewohnte Packung. Auch in diesem Fall werden morgens zwei Tabletten Kaftrio eingenommen.
Kinder ab 2 Jahre: Für Kinder zwischen zwei und fünf Jahren steht ein Granulat zur Verfügung. Dabei gibt es unterschiedliche Dosierungen für Kinder zwischen 10 und 14 kg Körpergewicht und 14 kg und mehr. Das Granulat wird z.B. mit etwas Flüssigkeit oder Joghurt/Pudding gemischt und soll dann mit einer fetthaltigen Mahlzeit eingenommen werden. Das Granulat muss nach dem Mischen innerhalb von einer Stunde eingenommen werden. Weitere Informationen finden Sie auch in der Packungsbeilage.
Tablette/Granulat vergessen?
Wenn Sie einmal eine Tablette vergessen haben, können Sie diese innerhalb von höchstens sechs Stunden noch einnehmen und mit dem ursprünglichen Plan weitermachen. Das gilt ebenso für das Granulat für Kleinkinder.
Wenn es mehr als sechs Stunden sind, ist es komplizierter, weil etwa zwölf Stunden zwischen der Morgen- und der Abenddosis vergehen sollen:
- Abenddosis vergessen: Fahren Sie ganz normal mit der nächsten Morgendosis fort.
- Morgendosis vergessen: Bitte nehmen Sie die Morgendosis noch ein, dafür dann aber die Abenddosis weglassen. Danach geht es wieder wie geplant mit der nächsten Morgendosis weiter.
Grundsätzlich sollten Sie zur Einnahme immer die Packungsbeilage lesen und sich bei Fragen an Ihren Arzt wenden.
Ich habe für mich entschieden, dass ich Kaftrio nehmen möchte. Was muss nun beachtet werden?
Kaftrio kann in Deutschland von Ärzten mit Erfahrung in der Behandlung von CF-Patienten verordnet werden. Die gesetzlichen Krankenkassen erstatten Kaftrio in Deutschland. Wenn die Verordnung innerhalb der Indikation gestellt wird (ab zwei Jahren und mindestens eine F508del-Mutation), sind keine zusätzlichen Anträge bei den gesetzlichen Krankenkassen notwendig.
Dokumentieren: welche CFTR-Mutationen liegen vor?
Der genetische Befund sollte auf jeden Fall schriftlich vorliegen, damit die ordnungsgemäße Verordnung nachgewiesen wird. Bei Unsicherheiten oder wenn der Befund schon länger zurückliegt, sollte man die Wiederholung des Tests erwägen.
Augenärztliche Untersuchung bei Kindern und Jugendlichen
Bei Kindern und Jugendlichen kann der Arzt vor und während einer Kaftrio-Behandlung die Untersuchung beim Augenarzt empfehlen. Denn in der Vergangenheit kam es bei einigen Kindern und Jugendlichen zu Linsentrübungen (Katarakt), die jedoch nicht zu einer Verschlechterung des Sehvermögens führten.
Regelmäßige Kontrolle von Blutdruck und Leberwerten
Der Hersteller hat weiterhin vorgegeben, dass alle Patienten, die Kaftrio erhalten, regelmäßig ihren Blutdruck kontrollieren lassen müssen, da Kaftrio den Blutdruck erhöhen kann. Auch die Leberwerte müssen regelmäßig kontrolliert werden, da Kaftrio die Leberfunktion stören kann.
Hinweise für die Verordnung:
Zwei Packungen
Kaftrio und Kalydeco müssen als zwei getrennte Präparate verschrieben werden. Das kann auf einem Rezept geschehen. Die Packung von Kaftrio mit 56 Tabletten reicht für 28 Tage. Dazu passt die Kalydeco-Packung mit 28 Tabletten, die ebenfalls 28 Tage lang reicht. Allerdings ist die Kalydeco-Packung mit 56 Tabletten kostengünstiger – die Verschreibung entsprechend wirtschaftlich. Wird die kleine Packung verordnet, sollte auch dies begründet werden (z.B. Gefahr der falschen Dosierung von Kalydeco).
Private Krankenversicherungen
Privat Versicherte haben grundsätzlich den gleichen Anspruch auf das Medikament wie gesetzlich Versicherte. Im Einzelfall kann die Kostenübernahme davon abhängen, welchen Tarif man gewählt hat. In jedem Fall ist es sinnvoll, vor Therapiebeginn die Kostenübernahme mit der privaten Krankenkasse zu klären.
Privat Versicherte müssen für das teure Medikament nicht unbedingt in Vorleistung treten. Man kann mit der Apotheke eine Abtretungserklärung vornehmen. Die Apotheke kann dann direkt mit der Krankenkasse abrechnen. Jede Apotheke müsste Vordrucke solcher Abtretungserklärungen vorliegen haben.
Bekommt man Kaftrio verordnet, sollten sich alle Beteiligten immer bewusst sein, dass es sich um ein extrem kostspieliges Medikament handelt. Die Therapie mit Kaftrio kostet im Monat so viel wie ein Kleinwagen, im Jahr so viel wie eine Immobilie. Das Wissen um diese hohen Kosten sollte Einfluss haben auf die zuverlässige Einnahme, die Durchführung der weiteren Therapien (Inhalation, Physiotherapie etc.) und den verantwortungsvollen Umgang mit dem Medikament. Und wenn Therapieziele nicht erreicht werden, man also merkt, dass das Medikament nicht oder unzureichend wirkt, sollte man auch über das Wiederabsetzen nachdenken.
Kann Kaftrio auch bei Patienten mit schlechtem Gesundheitszustand (u.a. eingeschränkte Lungen-, Leber- und Nierenfunktion) verordnet werden? Was ist zu beachten?
Wir haben die Informationen aus der Fachinformation dazu zusammen gefasst. Für weitere Informationen bitte Packungsbeilage beachten und bei Fragen ggf. an den Arzt wenden.
| Patientengruppe | Empfehlung |
| Patienten mit eingeschränkter Leberfunktion: | |
| Patienten sollen nicht mit Kaftrio behandelt werden. |
| Die Behandlung mit Kaftrio wird nicht empfohlen, kann aber u.U. in Erwägung gezogen werden. |
| Es ist keine Dosisanpassung empfohlen. |
| Patienten mit eingeschränkter Nierenfunktion: | |
| Es liegen keine Erfahrungen vor. Deshalb sollte die Anwendung mit Vorsicht erfolgen. |
| Es werden keine Dosisanpassungen empfohlen. |
| Patienten nach Organtransplantation | Die Anwendung von Kaftrio nach Organtransplantation wurde nicht untersucht. Die Anwendung ist deshalb nicht empfohlen. Zu beachten sind Wechselwirkungen mit Immunsuppressiva (s. Fachinformation). |
| Eingeschränkte Lungenfunktion (ppFEV1 < 40) | Diese Patientengruppe wurde in der Studie 445-102 untersucht. Sicherheit und Wirksamkeit unterschieden sich nicht von der Gesamtgruppe. |
Hilft Kaftrio auch nach einer Lungentransplantation – und für wen ist das Medikament sinnvoll?
In Deutschland darf Kaftrio auch nach einer (Lungen)transplantation verschrieben werden, obwohl das laut Fachinformation nicht empfohlen ist. Viele Menschen mit Mukoviszidose fragen sich deshalb, ob die Therapie nach einer Transplantation überhaupt sinnvoll ist – und für wen. Eine niederländische Studie (KOALA 2025) mit 55 Teilnehmenden ist diesen Fragen nachgegangen: Beschwerden der Nasennebenhöhlen und des Verdauungstrakts besserten sich deutlich, ebenso wie die Lebensqualität. Auch das Körpergewicht stieg leicht an. Der Langzeitblutzucker (HbA₁c) blieb hingegen trotz Kaftrio-Einnahme unverändert. Fünf Teilnehmende mussten die Behandlung wegen Nebenwirkungen abbrechen. Außerdem wurden die Medikamente gegen die Abstoßung des neuen Organs angepasst (wegen Wechselwirkungen mit Kaftrio). Da die Nierenwerte leicht anstiegen, wird empfohlen, diese engmaschig zu kontrollieren.
Fazit: Kaftrio kann auch nach einer Transplantation wirksam sein – insbesondere, um Probleme der Nasennebenhöhlen und Darmsymptomatik zu behandeln, erscheint dies sinnvoll. Voraussetzung ist jedoch immer eine sorgfältige ärztliche Begleitung.
Welche Alternativen gibt es für die, die nicht profitieren?
Es gibt Patienten, die Kaftrio wegen Unverträglichkeiten oder Wechselwirkungen mit anderen Medikamenten nicht nehmen können. Auch ist die Wirkung manchmal nicht gut und bei einigen seltenen Mutationen ist Kaftrio nicht zugelassen. Für diese Patienten gibt es weitere Forschung.
Weitere Informationen zur Verordnung von Kaftrio
Der Arzt darf innerhalb der Zulassung verordnen, muss aber in der Regel die kostengünstigste Alternative auswählen.
Hier ist die Nutzenbewertung durch den Gemeinsamen Bundesausschuss (G-BA) wichtig: Für jedes neue Medikament wird beim G-BA eine Bewertung durchgeführt, ob es besser wirkt als die bisher verfügbaren Vergleichstherapien. Bei Kaftrio wird dabei in mehrere Patientengruppen unterschieden, weil es bereits mehrere zugelassene Modulatoren (Vergleichstherapien) gibt. Die im Zusammenhang mit den Patientengruppen verwendeten Mutationsbezeichnungen (Minimalfunktionsmutation, Restfunktionsmutation, Gatingmutation) sind dabei nicht deckungsgleich mit den Mutationsklassen I-VI.
Nicht für alle Patientengruppen gibt es genug Studiendaten, um beim G-BA zeigen zu können, dass Kaftrio einen Zusatznutzen gegenüber den bisherigen Alternativen hat. Findet der G-BA keinen Zusatznutzen, kann die Verordnung von Kaftrio unwirtschaftlich sein und für den Arzt besteht evtl. ein Regressrisiko, d.h. die Krankenkasse könnte das Geld für das Medikament vom Arzt zurückfordern. Wir vom Bundesverband Mukoviszidose e.V. setzen uns dafür ein, dass Kaftrio für alle Patienten verordnet werden kann, für die es medizinisch sinnvoll ist.
Auf der folgenden Seite kann man alle Details zu den G-BA Beschlüssen nachlesen inklusive der Studiendaten (unter dem Buchstaben I findet man die verschiedenen Verfahren mit dem Wirkstoff "Ivacaftor" auf der 2./3. Seite):
Außerhalb der Zulassung können Einzelfallanträge an die Krankenkasse (off-Label-Anträge) gestellt werden.
Erfahrungsberichte
Tatjana kann Kaftrio aufgrund ihrer Mutation leider nicht nehmen. Wie es ihr damit geht, was sie sich für die Zukunft und vom Mukoviszidose e.V. wünscht, lesen Sie in unserem Bloginterview mit ihr.
Auch Jennifer kann kein Kaftrio nehmen, da sie eine seltene Mutation hat. Auch sie berichtet auf unserem Blog über ihr Leben mit CF und ohne Modulator.
Mehr zu HIT-CF und mutationsunabhängigen Therapien
- Gentherapie: was ist in Zukunft zu erwarten?
- Erste Phase des Hit-CF-Projekts erfolgreich abgeschlossen - 502 Patienten mit seltenen Mutationen haben teilgenommen
- Update Hit-CF: Leichte Verzögerung durch COVID-19, doch es geht weiter
- Neues von Hit-CF: Verzögerungen bei Studienteil – Erfolge im Labormodell
- Update HIT-CF: Klinische Studie mit neuen Modulatoren soll bald starten
Auswirkungen von Kaftrio auf Frauen und Männer
Schwangerschaft und Kaftrio

Die Daten im Deutschen Mukoviszidose-Register zeigen recht deutlich, dass es immer mehr Schwangerschaften bei Frauen mit Mukoviszdose gibt. Durch die teilweise Korrektur des zugrundeliegenden CFTR-Defektes durch Kaftrio kann also auch die reduzierte Fruchtbarkeit bei Frauen mit CF verbessert werden. Denn CFTR-Modulatoren wirken im ganzen Körper, nicht nur in der Lunge und der Bauchspeicheldrüse. Daher sollte man, falls man keinen Kinderwunsch hat, an Verhütung denken und mit seinem Arzt darüber sprechen. Während einer Schwangerschaft sollte die Weiterführung der Modulatortherapie individuell mit dem behandelnden Arzt abgewogen werden.
Weitere Informationen
Männer mit Mukoviszidose
Bei Männern mit Mukoviszidose ist in 98% kein Samenleiter ausgebildet. Es ist nicht zu erwarten, dass die Modulatoren hierauf einen Einfluss haben. Dennoch sind positive Auswirkungen der Therapie auf die männliche Gesundheit möglich.
Weitere Informationen
Hintergrundinformationen
Wie wirkt Kaftrio?
Kaftrio ist eine Kombination aus drei so genannten CFTR-Modulatoren: Elexacaftor, Tezacaftor und Ivacaftor. CFTR-Modulatoren reparieren teilweise den bei Mukoviszidose defekten CFTR-Salzkanal. Man unterscheidet Korrektoren und Potentiatoren. Korrektoren unterstützen den richtigen Zusammenbau des Salzkanals in der Zelle und sorgen so dafür, dass es immerhin Salzkanäle gibt, auch wenn sie nicht optimal funktionieren. Potentiatoren können solche Salzkanäle aktivieren und die Funktion verbessern.
Korrektoren: z.B. Elexacaftor, Tezacaftor
Potentiatoren: Ivacaftor, (Elexacaftor)
Ivacaftor (Kalydeco) ist ein solcher Potentiator, der die vorhandenen Kanäle aktivieren kann. Deshalb wirkt Kalydeco als Einzelwirkstoff auch nur bei Mutationen, bei denen noch Salzkanäle vorhanden sind, die aber nicht richtig arbeiten. Bei anderen Mutationen wirkt Kalydeco nur in Kombination mit Korrektoren, die dafür sorgen, dass die Salzkanäle gebildet werden. Elexacaftor und Tezacaftor sind die Korrektoren in Kaftrio. Sie helfen bei der Bildung des F508del-CFTR-Salzkanals. Kalydeco aktiviert diese Kanäle und verstärkt so den Effekt. Elexacaftor wirkt an einer anderen Stelle und unterstützt Tezacaftor. Inzwischen weiß man, dass Elexacaftor darüber hinaus auch eine Potentiator-Wirkung besitzt.
Grundsätzlich wirkt auch die Kombination aus Tezacaftor und Ivacaftor bei Patienten mit zwei F508del-Mutationen. Diese Zweifachkombination ist als Symkevi in Deutschland zugelassen. In Studien zeigte die Dreifachkombination aus Elexacaftor, Tezacaftor und Ivacaftor (Kaftrio) bei Patienten mit zwei F508del-Mutationen noch bessere Ergebnisse als die Zweifachkombination. Welches Medikament konkret verordnet wird, kann aber individuell unterschiedlich sein.
Wie oben gesagt, verstärkt das Kalydeco die Wirkung der anderen Wirkstoffe. Dass es zwei Packungen gibt, hat nur einen regulatorischen Hintergrund: Die Arzneimittelbehörde hat wegen einer möglichen Verwechslungsgefahr Bedenken, verschiedene Medikamente in einer Packung abzugeben. Kaftrio in Kombination mit Kalydeco entspricht also der in den Studien untersuchten Dosis und dem amerikanischen Trikafta.
Was ist neu an den CFTR-Modulatoren wie Kaftrio?
Diese neuen Medikamente reparieren (teilweise) den Salzkanal CFTR und greifen somit am Basisdefekt an. Sie beheben aber nicht die Ursache der Erkrankung, also den genetischen Defekt. Bisherige Therapien waren rein symptomatisch, d.h. es konnten nur die Krankheitszeichen (Symptome) behandelt werden.
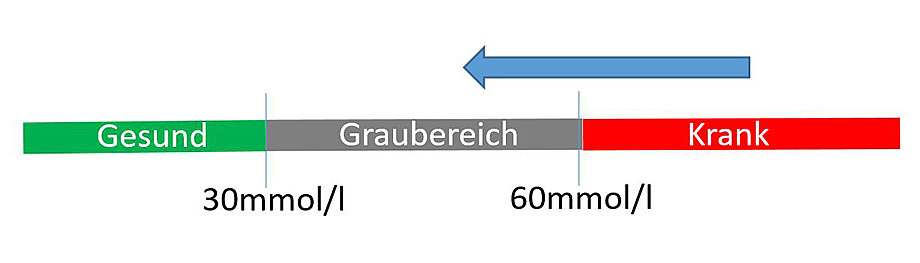
Dass Kaftrio einen direkten Effekt auf den CFTR-Kanal hat, sieht man auch an seiner Wirkung auf den Schweißtest, der sonst für die Diagnose der Mukoviszidose genutzt wird. Der Salzgehalt im Schweiß ist bei Patienten mit Mukoviszidose erhöht. Dies misst man im Schweißtest. Werte über 60mmol/l Chlorid (Salz) im Schweiß deuten auf eine Mukoviszidose hin; unter 30mmol/l Chlorid ist der Getestete gesund. Durch Kaftrio verschieben sich die Werte von durchschnittlich von „krank“ in den „Graubereich“. Patienten mit einem Schweißtestwert im Graubereich haben in der Regel mildere Krankheitsverläufe als Patienten mit höheren Salzwerten im Schweiß.
Ausblick: Werden Patienten, die Kaftrio nehmen, weniger Therapie machen müssen?
Kaftrio wird zweimal täglich als Tablette eingenommen. Allerdings muss die symptomatische Therapie, z.B. Physiotherapie, Inhalation, Ernährungstherapie u.a. weiterhin durchgeführt werden. Individuelle Anpassungen können ggf. sinnvoll sein. Das sollte aber immer mit dem behandelnden Arzt besprochen werden; keinesfalls sollte die Basistherapie unkontrolliert (ohne Rücksprache mit dem Arzt) abgesetzt werden.
In Studien wird systematisch untersucht, ob es sicher ist Begleittherapien nach Start einer Kaftrio-Behandlung abzusetzen: SIMPLIFY und CF STORM. Hier geht es konkret um die schleimlösenden Therapien mit hypertoner Kochsalzlösung und DNAse.
Erste Ergebnisse stimmen vorsichtig optimistisch: Die Simplify-Studie zeigte nach sechs Wochen keinen Unterschied zwischen der Gruppe mit mukolytischer Therapie und ohne. Allerdings wurden in dieser Studie auch nur Patienten mit einem sehr guten Gesundheitszustand untersucht (durchschnittlich 97% FEV1 bei Beginn der Studie) und die Studie dauerte eben auch nur wenige Wochen.
Die CF-STORM-Studie läuft über ein Jahr und will über 750 Patienten mit unterschiedlich guter Lungenfunktion aufnehmen. Die Ergebnisse werden dann voraussichtlich noch genauer Aufschluss darüber geben können, ob das Absetzen der mukolytischen Therapie (hypertone Kochsalzlösung bzw. DNAse) nach Start mit Kaftrio sicher ist und ggf. unter welchen Bedingungen.
Ausblick: Was sind die Langzeitwirkungen von Kaftrio?
Bei Kaftrio handelt es sich um eine Therapie, die lebenslang täglich eingenommen werden muss. Da das Medikament noch nicht lange zugelassen ist, sind Langzeitwirkungen, die sich vielleicht erst nach Jahrzehnten zeigen, noch unbekannt. Es werden jedoch Daten zu Wirksamkeit, Sicherheit und Nebenwirkungen erhoben.
Eine „Real World Data“ Auswertung zur Dreifachkombination (ETI) wurde anhand von Registerdaten aus dem Deutschen Mukoviszidose-Register und dem amerikanischen Register und für einen Zeitraum von zwei Jahren durchgeführt - ein wesentlich längerer Zeitraum, als in den Zulassungsstudien, in denen ein Zeitraum von 24 Wochen beobachtet wurde. Die Registerdaten zeigen: ETI verbessert die Lungenfunktion, führt zu weniger Krankenhausaufenthalten und die Keimbelastung nimmt ab. Die Ergebnisse wurden auch durch die Open-Label Studie, die den ETI-Zulassungsstudien angeschlossen wurden, bestätigt. Über einen Zeitraum von vier Jahren blieb die Lungenfunktion in dieser Studie stabil.
Podcast MUKO on Air
Links zum Thema Kaftrio
Unsere Newsmeldungen
- Zulassung von Trikafta in den USA
- EU: Dreifachkombination Elexacaftor/Tezacaftor/Ivacaftor steht vor der Zulassung
- Faktencheck zu Kaftrio
- Bevorstehende Zulassung von Kaftrio
- Zulassung von Kaftrio
- Gesundheitspolitik: G-BA sieht erheblichen Zusatznutzen von Kaftrio
- Kaftrio jetzt für Mukoviszidose-Patienten mit mindestens einer F508del-Mutation zugelassen
- So erleben Menschen mit Mukoviszidose die Therapie mit Kaftrio: eine systematische Befragung aus Frankreich
MUKOblog
- Erfahrungsberichte zu Kaftrio / Trikafta auf dem MUKOblog
- Interview mit Prof. Dr. Marcus Mall, Charité - Universitätsmedizin Berlin, zu Kaftrio
- Erfahrungsbericht mit dem Schwerpunkt Nebenwirkungen
- Interview mit Tatjana, die Kaftrio aufgrund ihrer Mutation leider nicht nehmen kann
- „Wir dürfen die Patienten nicht vergessen, die nicht von Kaftrio profitieren können“
- „Eine enge Zusammenarbeit des multidisziplinären Teams ist wichtig“
- Paradigmenwechsel in der CF-Ernährungstherapie: individualisierte Ernährungspläne und die Qualität der Nahrung rücken in den Fokus
- Kaftrio und andere Medikamente: Zusammentreffen in der Leber
- Erfahrungsbericht: Britta hat starke Nebenwirkungen durch Kaftrio
Quellen
Fachinformationen
Englischsprachige Produktinformation zu Kaftrio auf der EMA-Website inkl. einer Tabelle ("table 5") mit den Mutationen, für die Kaftrio zugelassenen ist:
Weitere Quellen
Burgel PR, Girodon E, Sharma N, Raynal C, Da Silva J, Sasorith S, Martin C, Sermet-Gaudelus I, Raraigh K. (2025) Elexacaftor-tezacaftor-ivacaftor in people with cystic fibrosis harbouring two CFTR Class I variants: real-world data from the French compassionate programme. EClinicalMedicine. 2025 Aug 30;88:103476. doi: 10.1016 Zum Artikel
Heijermann et al. (2019) Efficacy and safety of the elexacaftor plus tezacaftor plus ivacaftor combination regimen in people with cystic fibrosis homozygous for the F508del mutation: a double-blind, randomised, phase 3 trial, In: The Lancet; 394 (10212): 1940-1948. Zum Artikel
Middleton et al. (2019) Elexacaftor–Tezacaftor–Ivacaftor for Cystic Fibrosis with a Single Phe508del Allele. In: N Engl J Med 2019; 381:1809-1819. Zum Artikel
Zemanick et al. (2021) A Phase 3 Open-Label Study of Elexacaftor/Tezacaftor/Ivacaftor in Children 6 through 11 Years of Age with Cystic Fibrosis and at Least One F508del Allele, In: Am J Respir Crit Care Med 203(12): 1522-1532. Zum Artikel
KOALA study group; van Gemert JP, Luijk B, Hellemons ME, Visser KA, Hansen CME, van der Meer R, Gan CT, van der Vaart H, Akkerman OW, Steenhuis WN, Verkleij M, Heijerman HGM, Verschuuren EAM. Evaluation of Elexacafor/Tezacaftor/Ivacaftor therapy after lung transplantation in Cystic Fibrosis: The Dutch National KOALA study. JHLT Open. 2025 Jan 17;7:100210. doi: 10.1016/j.jhlto.2025.100210. PMID: 40144832; PMCID: PMC11935345. Zum Artikel
Die Inhalte auf dieser Seite wurden zuerst im März 2020 erstellt.

