Vorherige Nutzenbewertungen von Kaftrio für Patienten ab 12 Jahren heterogen
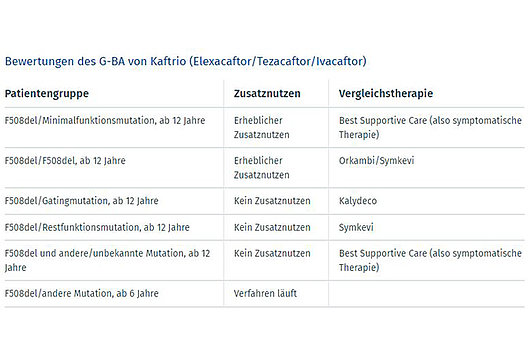
Die Bewertungen des Zusatznutzens von Kaftrio für die verschiedenen Patientengruppen sind aufgrund sehr unterschiedlicher Datenqualität sehr verschieden. Für Menschen mit Mukoviszidose über 12 Jahre und mit zwei F508del-Mutationen, bzw. einer F508del in Kombination mit einer Minimalfunktionsmutation, wurde ein „erheblicher Zusatznutzen“ vergeben, eine sehr positive Bewertung, die die guten internationalen Erfahrungen mit Kaftrio widerspiegelt. Bei den selteneren Gatingmutationen, Restfunktionsmutationen und allen anderen Mutationen in Kombination mit F508del wurde hingegen kein Zusatznutzen festgestellt (s. Tabelle). Das bedeutet aber keineswegs, dass Kaftrio bei diesen Mutationen nicht individuell einen (großen) Nutzen haben kann. Ein Zusatznutzen konnte lediglich nicht abgeleitet werden, da die vorgelegten Studien zu kurz waren oder es gar keine Studien gab.
Ähnliches Bild bei Kindern zwischen 6 und 11 Jahren
Bei Kindern zwischen 6 und 11 Jahren ist die Situation ähnlich. Für die Mutationskombination F508del und Minimalfunktionsmutation gibt es eine gute klinische Studie, von der man laut IQWiG einen Anhaltspunkt auf einen beträchtlichen Zusatznutzen ableiten kann. Für F508del/F508del gibt es leider nur eine einarmige Studie, d.h. es wurde kein Vergleich mit einem Scheinmedikament (Placebo) oder einem anderen CFTR-Modulator durchgeführt. Deshalb kann man rein formal hier nur schwer einen Zusatznutzen ableiten. Für alle anderen Mutationsgruppen wurden keine Studien durchgeführt und das IQWiG findet entsprechend auch keinen Zusatznutzen. Wie erwähnt, muss der G-BA dieser Einschätzung aber nicht folgen. Der G-BA bezieht u.a. noch Expertenvoten mit in seine Entscheidung ein.
Stellungnahmefrist für Experten bis zum 07. Juni
Medizinische Sachverständige sind aufgerufen, zu den IQWiG-Bewertungen Stellung zu nehmen. Diese Fachvoten gehen in die Bewertung des G-BA ein. Patienten und Patientenvertreter dürfen übrigens ausdrücklich keine Stellungnahmen einreichen, da sie über die formale Patientenvertretung in die G-BA Verfahren eingebunden sind. Auch der Mukoviszidose e.V. darf regelmäßig (nicht stimmberechtigte) Patientenvertreter in die für Mukoviszidose relevanten Verfahren entsenden (über den deutschen Behindertenrat und die BAG Selbsthilfe). Die Einreichungsfrist für Experten läuft noch bis zum 07. Juni 2022. Eine mündliche Anhörung erfolgt am 27. Juni 2022; der Beschluss soll Anfang August getroffen werden.
Mögliche Auswirkungen der G-BA Entscheidung auf die Verordnungsfähigkeit
Findet der G-BA keinen Zusatznutzen, ist dies zwar ausdrücklich kein Verordnungsausschluss (Therapiefreiheit des Arztes), aber Verordnungen müssen auch wirtschaftlich sein. Deshalb muss insbesondere bei fehlendem Zusatznutzen jeder Einzelfall sorgfältig begründet und am besten mit Daten belegt werden, denn es kann ggf. zu Prüfungen der Verordnung kommen.
Weitere Informationen
Information des G-BA zu den Verfahren (inkl. Link zu den IQWiG Nutzenbewertungen und Stellungnahme-Möglichkeiten):
- F508del/F508del: G-BA Nutzenbewertung 801 und G-BA Nutzenbewertung 794
- F508del/MF-Mutation: G-BA Nutzenbewertung 800 und G-BA Nutzenbewertung 793
- F508del/Gating-Mutation: G-BA Nutzenbewertung 802 und G-BA Nutzenbewertung 795
- F508del/Restfunktionsmutation: G-BA Nutzenbewertung 803 und G-BA Nutzenbewertung 796
- F508del/andere bzw. unbekannte Mutation: G-BA Nutzenbewertung 804 und G-BA Nutzenbewertung 797
Bei Fragen wenden Sie sich bitte an Dr. Jutta Bend (jbend(at)muko.info).
In diesem Beitrag werden Wirkungen bzw. Nebenwirkungen von Arzneimitteln besprochen. Diese Informationen werden durch das Mukoviszidose-Institut ohne den Einfluss Dritter nach bestem Wissen und Gewissen bereitgestellt. In keinem Fall ist damit eine Empfehlung für den Gebrauch oder Nichtgebrauch eines Arzneimittels verbunden. Patienten sollten vielmehr mit ihrem Arzt/ihrer Ärztin individuell die für sie in Frage kommenden Therapieoptionen besprechen.